【解説】初の国産…塩野義製薬の飲み薬「見送り」に “緊急承認”申請も「データ不足」指摘する声相次ぐ
新型コロナウイルスの感染が第7波に入り、医療機関のひっ迫も懸念される中、注目されていた初の「国産飲み薬」の承認の判断が見送られました。
「見送り決定“舞台裏”」「症状改善に“ほぼ効果ない”」「既存薬はBA.5に効果」以上の3つのポイントについて詳しく解説します。
全国の新規感染者は20日、15万2536人と過去最多になりました。都道府県別では、30の府と県で過去最多を更新し、大阪では初めて2万人を超えました。
関係者によると、東京の21日の感染者は、3万1878人となることが分かっています。全国の重症者は20日時点で189人となり、再び増加しています。
今回の第7波は、感染者の増加のスピードが急激な点が懸念されています。こうした中、期待されているのが、自宅で簡単に服用できる飲み薬です。
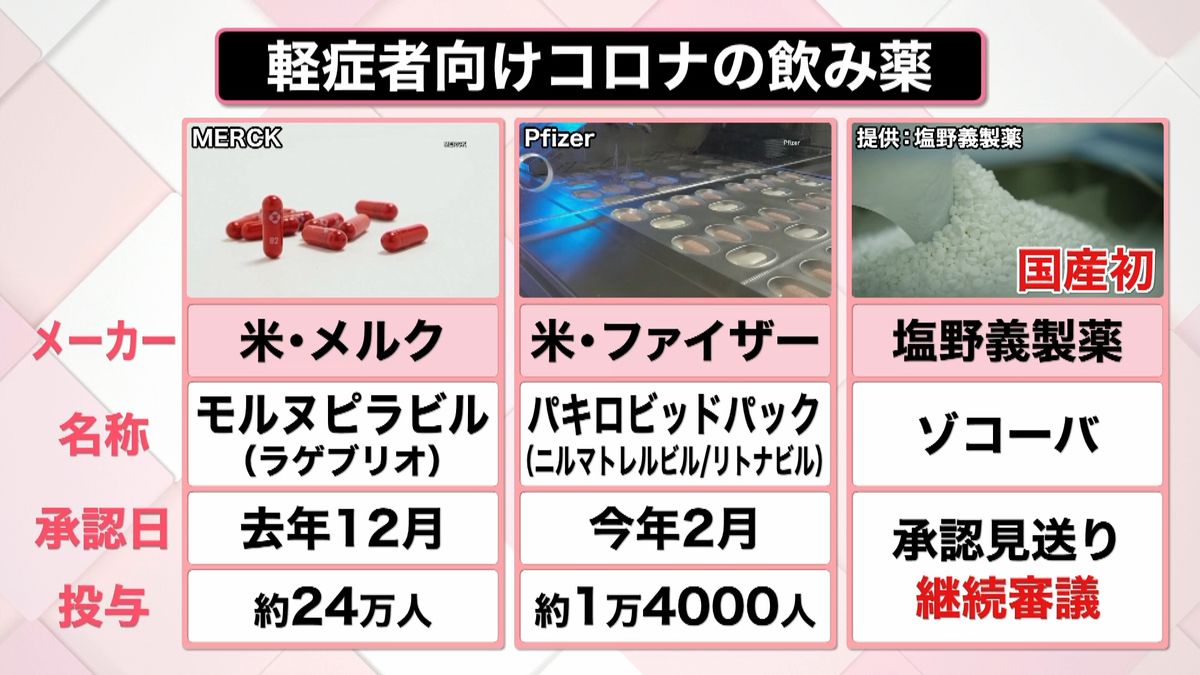
現在、国内で承認されている軽症者向けの飲み薬は、アメリカのメルクが開発した「モルヌピラビル」。こちらは去年12月に特例承認され、約24万人に投与されています。また、アメリカのファイザーの「パキロビッドパック」は、今年2月に特例承認され、約1万4000人に投与されています。
この2つに続いて、第三の軽症者向け飲み薬として注目されているのが、塩野義製薬が開発した国産初の飲み薬「ゾコーバ」です。この薬は国産というところがポイントで、海外の事情に左右されず、国内での安定供給が期待されているというものです。
この薬について20日、厚生労働省の専門部会は承認の判断を見送り、「継続審議」としました。今後、完全に承認への道が閉ざされたというわけではなく、承認される可能性は残っています。
今回、なぜ承認の判断が見送られたのでしょうか。
専門家からは厳しい意見が相次ぎました。20日に2時間にわたって行われた専門部会で、委員らからは「最終段階の臨床試験の結果が出るまでは、とても使えない」などとデータ不足を指摘する声が相次ぎました。
そして、「提出されているデータから『有効性が推定される』という判断はできない」との意見が多くを占め、結局、全会一致で承認の判断を見送ることとなりました。つまり、今あるデータでは効果を証明できないので、継続して審議をしていくという判断になったわけです。
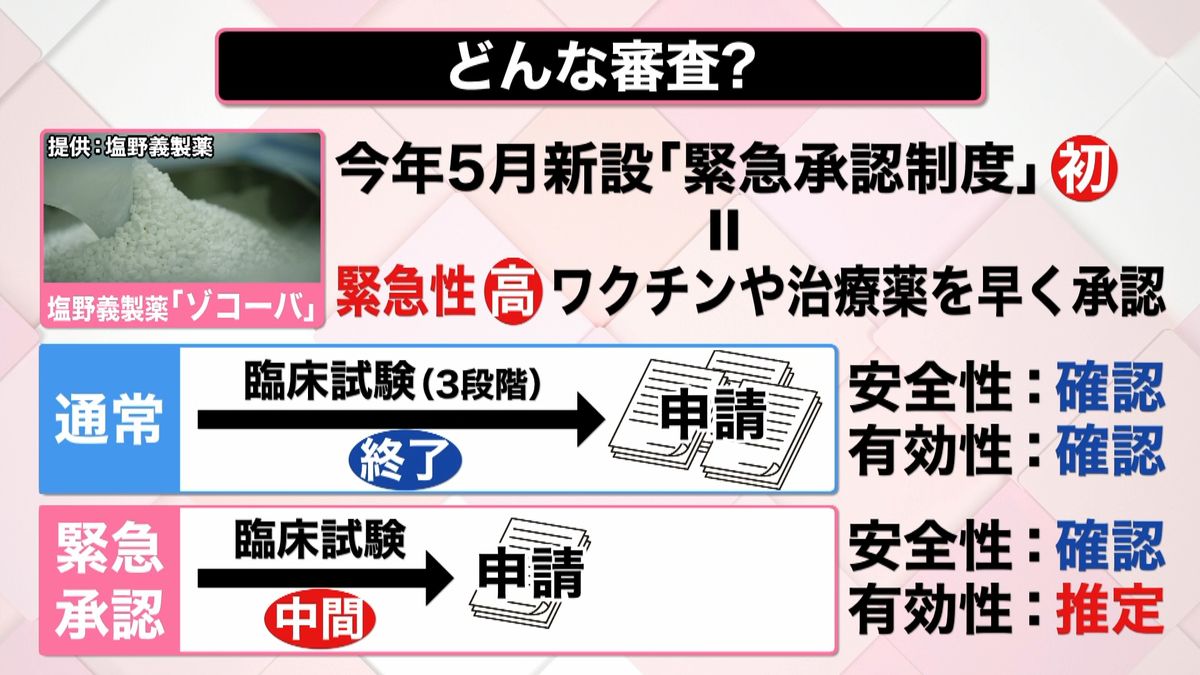
そもそも、今回の審査は通常の承認制度ではなく、今年5月にできた「緊急承認制度」を使った初めてのケースでした。
この制度は、新型コロナなど緊急性の高いパンデミックなどの際に、ワクチンや治療薬を通常より早く承認し実用化するためにできたものです。
通常は3段階の臨床試験が終わって、全てのデータが出そろってから承認を申請することになりますが、緊急承認制度では臨床試験が全て終わっていなくても、中間段階のデータでの承認申請が可能になります。
そして、安全性についてはこれまで通り「確認」が必要ですが、有効性については「推定」できれば暫定的に承認するという仕組みです。「ある程度、効果がありそうだな」と推定できれば、承認されるということになります。
つまり、通常より合格のハードルを下げたにもかかわらず、今回は「有効性が推定できるとは判断できない」との結論に至りました。
なぜ、このような判断になったのでしょうか。
医薬品を審査する機関「PMDA」の報告書では、「ゾコーバ」について、「ウイルスが減少する効果は確認できているものの、新型コロナの12症状の改善状況については、基準を満たしていない」と評価されています。
つまり、薬を投与した集団と投与していない集団で比較したところ、ほとんどの症状で回復の傾向が「ほぼ同じ」推移を示していたということです。
飲んでも、飲まなくても回復にはほぼ差はなかったということで、審査機関の委員は「ほぼ結果に効果がないと見える」と説明しました。
現在、承認されているメルクの「モルヌピラビル」とファイザーの「パキロビッドパック」では、入院や死亡リスクをそれぞれ3割減少、約9割減少させることが確認されています。
それに比べると、塩野義製薬の「ゾコーバ」では症状の改善に効果がみられないため、有効性があると推定するには至らなかったということです。ほかにも、基礎疾患の薬との併用ができないことや、妊婦などに投与が難しいことも、承認が見送られた背景にあります。
ただ、オミクロン株は軽症者が多く、すぐに症状が改善する人が多いです。そのため、前の2つ薬が承認された時に比べ、薬の効果を証明するのが難しくなっているという点も指摘されています。
今回の結果について、感染症・呼吸器疾患が専門の加藤哲朗医師は「『しっかりとしたデータを見極めた上で承認する』というプロセスを取ろうとしたことが分かる。効果が確認できないものを承認するのはリスクが高く、焦らずやるべき。今後、十分なデータが出た段階で、しっかり評価されることを期待したい」と話していました。
国内で承認されている2つの飲み薬と点滴で投与するレムデシビルについて、東京大学などの研究によると、現在、置き換わりが進むBA.5に対して、BA.2よりもウイルスの増殖を抑える効果が高いことが分かったということです。安心材料の1つになるかもしれません。
◇
今後、塩野義製薬は最終段階の臨床試験の結果など新たなデータを提出し、再び審査を受けることになります。一方で、加藤医師は「飲み薬さえあれば大丈夫ということではない」と話しています。「基本的な感染対策とワクチン接種、それでも感染したら薬を投与と、3つを並列で考えることが大切」だと強調していました。
(2022年7月21日午後4時半ごろ放送 news every. 「知りたいッ!」より)